融合基因在血液肿瘤的诊断、预后、分层以及治疗中均起到重要作用。WHO在2000年发布的白血病和淋巴瘤诊断标准已将染色体易位后融合基因检测作为重要的指标之一,用于治疗方案的确定以及预后分析。
随着分子技术尤其是高通量测序技术的发展,大量的血液肿瘤相关的少见融合基因被发现。目前临床上融合基因检测仅能针对最常见的数十种融合进行检测,覆盖种类尚不足10%,依然存在患者未能准确分层,遭遇过度治疗或治疗不足的情况。对于血液肿瘤患者而言,准确的预后分层是临床治愈率能否进一步提高的关键。
如果曾经临床上对如此多变的融合基因检测覆盖不全“是不能也,非不为也”,那么优睿®血液肿瘤融合基因检测的出现将全面扭转这种被动局面。
背 景
● 血液肿瘤的治疗与分层密不可分
血液肿瘤主要包括各类白血病、多发性骨髓瘤以及恶性淋巴瘤。目前国际上采用MICM诊断和分型标准,即综合形态检测(Morphology)、免疫检测(Immunology) 、细胞遗传学检测(Cytogenetics)以及分子检测(Molecular)的结果对患者进行诊断、分型及分层。在MICM精准分型与分层的基础上,选择最有效的治疗方案,实现精准治疗。
● 融合基因对预后分层至关重要
随着分子生物学技术的发展,对于血液肿瘤的检测深入到分子层面。大家逐渐认识到大部分的血液肿瘤中存在着染色体结构畸变(包括缺失、重复、倒位、易位等),会导致融合基因的产生以及融合蛋白的编码。而这些融合基因在血液肿瘤的诊断、预后、分层以及治疗中均起到重要作用。
如BCR-ABL融合基因,可出现在95%以上的慢性粒细胞白血病中(CML)。急性早幼粒细胞白血病(APL)特有的PML-RARa融合基因,用全反式维甲酸(ATRA)诱导缓解治疗,其预后非常好,复发率低。而有些融合,如MLL相关融合基因,预后差,死亡率高。
● 目前常用融合基因检测恐难满足临床需求
迄今为止报道的融合基因已有千种。仅在一项179例AML患者的NGS研究中,就检测到了118个融合基因。而在另一项2345例存在MLL基因重排的白血病患者中,通过长片段PCR+测序检测到MLL的融合伴侣种类多达135种。临床融合基因检测中覆盖种类尚不足10%。而许多少见的融合基因依旧具有明确的临床价值和意义。
基于AMLSG及Mitelman数据库,下表展示了部分少见融合基因及其对于预后的影响。
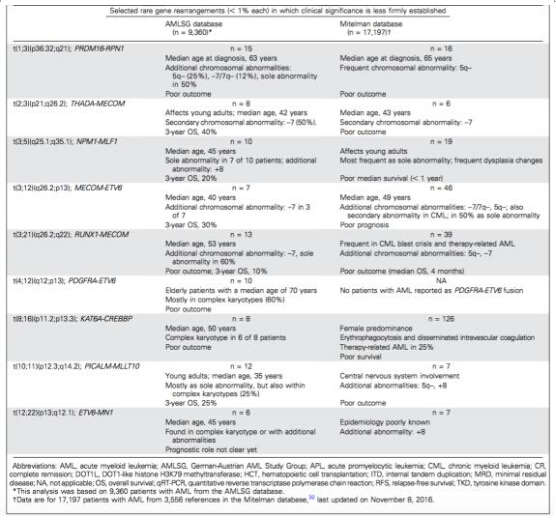
▲Bullinger, Lars, Konstanze Döhner, and Hartmut Döhner. Journal of Clinical Oncology 35.9 (2017): 934-946.
除了对预后/危险度的精准分层外,融合基因也会对诊断、靶向治疗给予更全面的提升,如在一项154例ph-like B-ALL患者的研究中,62%的患者检出了35种激酶相关的融合基因。其中JAK2(10种)、ABL1(6种)、PDGFRB(4种)、ABL2(3种)。而在这类携带激酶类重排的患者,采取相应的激酶抑制剂进行靶向治疗,已经有多项此类的临床试验在进行。

▲Hematopathology. 2016;1(1):11-15
● 传统融合基因检测方法技术有限
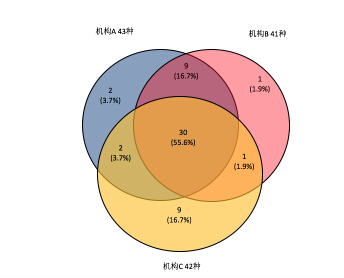
为何目前临床融合基因检测仅仅检查数十种融合基因呢?而且在整理临床常用的3家融合基因检测机构的筛查范围,发现三者共同筛查的融合的比例仅为55.6%。究其原因,乃是检测技术限制所致。
具体说来目前临床上均是基于多重PCR或荧光PCR原理的融合基因检测解决方案。此类解决方案需要针对每个融合类型(一种融合基因含有多种融合类型)进行特异的引物设计。引物设计以及反应体系要求随着同时检测的融合断点数目增加而增加,因此造成了检测通量上不去,检测范围有差异的现状。
优睿®血液肿瘤融合基因检测大有可为
为让临床能更精准更全面的检测融合基因,优迅医学研发了结合新一代高通量测序技术(NGS)与探针富集技术的融合基因检测方案,突破了PCR融合基因检测只能检测已知融合位点的限制,避免了多重PCR引物设计的约束,将检测通量提高20倍,真正实现了融合基因的全面检测,从而将最新的临床研究成果迅速转化至临床,实现更加精准的诊断与预后/危险度分层,帮助患者选择更有效的治疗方案,达到最大的临床获益。
● 优睿®血液肿瘤融合基因标准套餐 ●
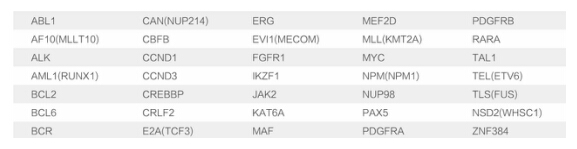
500+融合(35核心基因)
根据融合基因的发生频率及融合伴侣数目,精选35个血液肿瘤核心基因,涉及已知融合518种。
● 优睿®血液肿瘤融合基因标准套餐 ●
900+融合(225基因)
整合NCCN、ELN等指南、权威数据库及最新科研成果,一次性检测900+种融合基因,实现融合基因全覆盖。

适用人群
● 疑似或初诊的血液肿瘤患者
● 形态学缓解前未做过融合基因筛查的血液肿瘤患者
● 传统方法未检测到融合基因的血液肿瘤患者
● 治疗效果不佳的血液肿瘤患者
优睿®血液肿瘤融合基因检测可为以上患者提供预后及危险度分层的精准评估、血液肿瘤的辅助诊断及分型分层、靶向药及治疗方案(化疗、移植等)的决策支持、难治/复发患者病因查询。
检测周期:自实验室接收到样本起,12个工作日。
贴心服务:若检测到频率低于2%的融合基因,优迅医学提供免费验证(报告周期顺延)。
重要优势
√ 从根本上解决了常见融合因融合断点造成的漏检,相同检测范围下的性能提升。
√ 检测通量提高20倍,涵盖了已报道的全部融合,且部分拓展到未知融合,检测范围大幅提升。
√ 互补核型检测结果,降低由于核型主观性以及其他技术原因导致的假阴性结果。
√ 通过检测范围以及性能的大幅提升,最终使得危险度分层更加精准,从而选择更有效的治疗方案。
√ 增大了检出微残检测(MRD)靶点的可能性。
优睿在多大程度上帮助解决了临床上检测不足的问题?
● 大幅提高危险度分层准确率
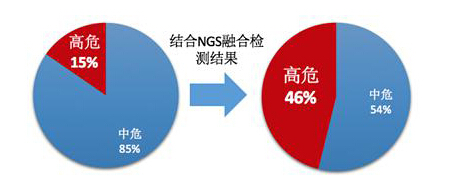
优迅医学对65例(常规融合检测阴性)临床回顾性样本进行NGS优睿®融合基因检测,共在19例样本中检测到融合基因,检出比例达到29%。对于26例难治患者的危险度分层准确率,由15%提升至46%。这就意味着对比传统融合基因检测方法,8名患者(30%)会受益于优睿®融合基因检测,得到准确的危险度分层,从而调整治疗方案。
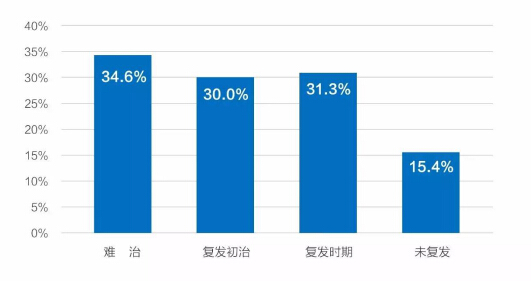
不同预后组别检出率
● 大幅降低核型检测假阴性情况
染色体核型作为目前各大指南危险度分层的重要指标,但由于敏感性以及技术原因会出现一定的假阴性结果,从而误导临床诊疗。而优睿®融合基因检测可互补核型检测,降低核型检测的假阴性情况。通过对34例核型正常的回顾性样本进行优睿®融合基因检测,12例(35%)患者NGS融合基因检测为阳性,从而提示该样本的染色体存在易位。下图为漏检核型示例,该患者MLL-SEPT9融合阳性,其对应核型应为t(11;17)(q23;q25) 。

参考文献:
[1] Bullinger, Lars, Konstanze Döhner, and Hartmut Döhner. Journal of Clinical Oncology 35.9 (2017): 934-946.
[2] Meyer, C., et al. Leukemia 27.11 (2013): 2165.
[3] Cancer Genome Atlas Research Network. N Engl j Med 2013.368 (2013): 2059-2074.
[4] Tran, Thai Hoa, and Mignon L. Loh. Hematology. American Society of Hematology. Education Program 2016.1 (2016): 561-566.
[5] Roberts, Kathryn G., et al. New England journal of medicine 371.11 (2014): 1005-1015.